Soal Kimia Kelas 12 Bab 5 Korosi ~ sekolahmuonline.com
Soal Kimia Kelas 12 Bab 5 Korosi ~ sekolahmuonline.com. Pembaca Sekolahmuonline, berikut ini Sekolahmuonline posting contoh soal pilihan ganda atau multiple choice mata pelajaran Kimia kelas 12 Bab 5 yang membahas tentang Korosi. Silahkan dibaca dan dipelajari, semoga membantu memudahkan Anda khususnya mamas-mamas dan mbak-mbak yang sedang belajar Kimia secara mandiri di rumah khususnya pembahasan Bab Korosi.
Kimia Kelas XII Bab 5 Korosi sbagaimana telah Sekolahmuonline sampaikan pada Rangkuman Kimia Kelas 12 Bab Korosi membahas dua kegiatan pembelajaran, yaitu:
- Pertama: Faktor-faktor yang mempengaruhi proses korosi
- Kedua: Cara mengatasi korosi
Soal Kimia Kelas XII Bab 5 Korosi
A. Soal Pilihan Ganda Kimia Kelas 12 Bab 5 Korosi
Jawablah soal-soal berikut ini dengan memilih huruf A, B, C, D, atau E pada jawaban yang benar dan tepat!
1. Mudah atau tidaknya logam berkarat tergantung pada …
A. Banyaknya air
B. Kereaktifan logam
C. Suhu lingkungan
D. Tingkat kebasaan
E. Banyaknya oksigen
Kunci Jawaban: B
Pembahasan:
Pertanyaan nomor 1 terkait kecenderungan logam dalam mengalami perkaratan atau reaksi oksidasi bukan terkait faktor yang mempercepat terjadinya perkaratan. Kecenderungan suatu logam dalam mengalami oksidasi bergantung dari besar kecil nilai potensial reduksi logam tersebut. Semakin kecil potensial reduksi logam, maka semakin mudah logam mengalami oksidasi atau semakin reaktif
2. Berikut ini yang merupakan faktor-faktor penyebab terjadinya korosi adalah …
A. Air dan oksigen
B. Oksigen dan tanah
C. Tanah dan minyak
D. Minyak dan larutan asam
E. Minyak dan air
Kunci Jawaban: A
Pembahasan:
Faktor-faktor penyebab terjadinya korosi adalah:
- Gas oksigen
- Air
- Zat asam
- Zat elektrolit
3. Faktor-faktor yang berasal dari lingkungan berikut ini dapat mempengaruhi korosi kecuali . . . .
A. Suhu
B. Udara
C. Keasaman
D. Kelembaban
E. Struktur bahan
Kunci Jawaban: E
Pembahasan:
Faktor-faktor penyebab terjadinya korosi adalah:
- Gas oksigen terdapat pada udara
- Air menentukan kelembaban.
- Zat asam memiliki ion H+ sebagai katalis dalam perkaratan.
- Zat elektrolit
Struktur bahan kondisi tata letak partikel-partikel dari bahan, hal ini tidak mempengaruhi proses perkaratan.
4. Dalam proses perkaratan besi, besi bertindak sebagai …
A. katoda
B. anoda
C. katalis
D. jembatan garam
E. elektrolit
Kunci Jawaban: B
Pembahasan:
Dalam perkaratan besi, besi mengalami oksidasi, sehingga besi bertindak sebagai anoda
5. Berdasarkan reaksi redoks pada proses perkaratan, lingkungan seperti apa yang menyebabkan besi mudah berkarat?
A. kering
B. lembab
C. vakum
D. berminyak
E. panas
Kunci Jawaban: B
Pembahasan:
Lingkungan yang menyebabkan besi mudah berkarat adalah lingkungan yang kondisinya mengandung faktor-faktor yang mempercepat reaksi perkaratan.
- kering : lingkungan kering diasumsikan sedikit mengandung uap air.
- lembab : lingkungan basah diasumsikan banyak mengandung uap air.
- vakum : lingkungan vakum diasumsikan tidak mengandung gas oksigen.
- berminyak : lingkungan berminyak dapat menutup permukaan logam sehingga tidak kontak dengan lingkungan luar.
- panas: lingkungan panas dapat menyebabkan uap air menguap atau berkurang dari sekitar logam.
6. Jika diketahui larutan A, B, C, D dan E berturut-turut mempunyai pH = 4, 6, 7, 8 dan 9, manakah dari larutan tersebut yang paling cepat menyebabkan perkaratan pada besi?
A. Larutan A
B. Larutan B
C. Larutan C
D. Larutan D
E. Larutan E
Kunci Jawaban: A
Pembahasan:
Dalam reaksi perkaratan ion H+ adalah spesi yang bertindak sebagai katalis, jadi semakin kecil pH semakin banyak mengandung ion H+.
7. Diketahui gambar percobaan tentang korosi besi berikut:
Catatan :
- Air mendidih mengandung lebih sedikit gas oksigen terlarut.
- Senyawa anhidrat mempunyai sifat mudah menyerap air.
Berdasarkan data tersebut urutan terbentuknya korosi dari yang paling cepat adalah .. . .
A. 1 – 2 – 4 – 3
B. 2 – 1 – 4 – 3
C. 3 – 1 – 2 – 4
D. 3 – 4 – 1 – 2
E. 4 – 2 – 1 – 3
Kunci Jawaban: B
Pembahasan:
Larutan H2SO4 karena bersifat asam. Kita tahu pH < 7 akan mempercepat terjadinya reaksi korosi karena adanya reaksi reduksi tambahan dari ion H+ yang berasal dari asam.
Air. Karena air mengandung banyak oksigen terlarut yang mempercepat terjadinya korosi.
Air yang didihkan. Karena jumlah oksigen terlarut dalam air manjadi sedikit CaCl2 dan udara kering. Kristal CaCl2 anhidrat berfungsi sebagai media yang dapat menyerap uap air yang ada di udara sehingga memperkecil kontak dengan paku
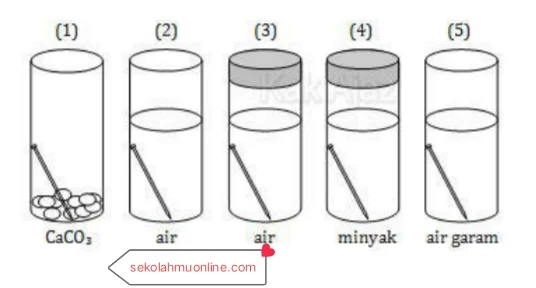
8. Perhatikan gambar proses korosi berikut!
Proses korosi yang berlangsung paling lambat adalah ….
A. 1
B. 2
C. 3
D. 4
E. 5
Kunci Jawaban: D
Pembahasan:
Keterangan masing-masing gambar pada nomor 8 di atas adalah sebagai berikut:
1) Paku berada pada tabung terbuka sehingga O2 dapat masuk. Tetapi di dalam tabung terdapat CaCO2 yang bersifat menyerap H2O sehingga udara tetap kering. [lambat korosi]
2) Paku berada pada tabung terbuka yang berisi air atau paku berada pada medium yang mengandung O2 dan H2O [cepat korosi]
3) Paku berada pada tabung tertutup yang berisi air. Meskipun tabung tertutup tetapi di dalamnya masih tersisa udara sehingga masih memungkin paku berkarat. [agak lambat korosi]
4) Paku berada pada medium tertutup yang berisi minyak. Berarti jumlah O2 dalam tabung terbatas dan H2O tidak dapat menembus minyak. [sangat lambat korosi]
5) Paku berada pada tabung terbuka yang berisi air garam. Sedangkan air garam bersifat elektrolit yang dapat mempercepat reaksi oksidasi. [sangat cepat korosi]
9. Salah satu kelebihan pencegahan perkaratan pada besi dengan cara pengecatan adalah…
A. Tidak bisa rusak.
B. Tidak mudah patah.
C. Tidak mudah terbakar.
D. Mempunyai nilai estetika.
E. Tidak mudah tergores.
Kunci Jawaban: D
Pembahasan:
Kelebihan pengecatan adalah untuk pencegahan perkaratan besi dan menambah nilai estetika
10. Berikut tentang cara pencegahan perkaratan dengan cara pelapisan logam menggunakan logam krom (Cr) kecuali …
A. Dilakukan dengan elektrolisis.
B. Tidak mudah berkarat.
C. Memberikan penampilan mengkilat.
D. Biasa digunakan untuk melapisi bamper mobil.
E. Besi tidak berkarat meskipun sebagaian lapisan crom rusak.
Kunci Jawaban: E
Pembahasan:
Chrome plating (pelapisan dengan krom)
Krom (Cr) memberi lapisan pelindung, sehingga besi yang sudah diberi lapisan krom akan mengkilap. Pelapisan dengan krom ini dilakukan dengan proses elektrolisis. Krom juga dapat memberikan perlindungan meskipun pada suatu lapisan krom tersebut ada yang rusak.
11. Salah satu kelemahan pada cat berbahan dasar minyak adalah…
A. Mudah terbakar.
B. Mudah berkarat.
C. Lengket.
D. Mudah meleleh.
E. Mudah patah.
Kunci Jawaban: A
Pembahasan:
Minyak mempunyai sifat mudah terbakar
12. Pencegahan perkaratan menggunakan pelumuran oli atau minyak lebih cocok untuk benda....
A. Gear pada mesin motor.
B. Pagar.
C. Kompor.
D. Kawat.
E. paku
Kunci Jawaban: A
Pembahasan:
Pelumuran dengan oli untuk mencegah perkaratan lebih cocok untuk alat-alat bagian dalam dari permesinan.
13. Berikut tentang cara pencegahan perkaratan dengan cara pelapisan logam menggunakan logam timah (Sn) kecuali …
A. Biasa untuk melapisi kaleng.
B. Memberikan lapisan yang tahan karat.
C. Dilakukan dengan elektrolisis.
D. Besi tetap tahan karat walau sedikit lapisan timah rusak.
E. Memberikan warna mengkilat.
Kunci Jawaban: D
Pembahasan:
Tin plating (pelapisan dengan timah)
Lapisan pada timah akan melindungi besi selama lapisan itu masih utuh. Apabila terdapat goresan, maka timah ini justru mempercepat suatu proses korosi karena potensial elektrode timah lebih positif dari besi.
14. Berikut cara yang paling jitu untuk menyimpan paku besi agar tidak mudah berkarat adalah dengan....
A. Diletakkan dalam kantung kain.
B. Dijemur.
C. Direndam air.
D. Disimpan dalam kaleng seng.
E. Disimpan dalam guci tembaga.
Kunci Jawaban: D
Pembahasan:
Untuk menyimpan paku, kita upayakan dengan cara gampang dan murah. Tidak perlu mengupayakan dengan reaksi kimia. Cukup dengan menghindarkan paku dari faktor penyebab perkaratan diantaranya gas oksigen, air, larutan elektrolit, permukaan besi.
Kantung kain masih memungkinkan kontaknya paku dengan pemacu perkaratan, demikian juga dengan dijemur atau direndam air.
Jika disimpan dalam guci tembaga, maka akan cenderung terjadi oksidasi besi (paku) karena besi mempunyai potensial reduksi lebih kecil dari tembaga.
Jika disimpan dalam kaleng seng (Zn), maka akan terjadi oksidasi seng, karena seng mempunyai potensial reduksi lebih kecil dari besi.
15. Pada Teknik perlindungan katodik, logam besi yang dilindungi bertindak sebagai …
A. Katoda
B. Anoda
C. Elektrolit
D. Penghantar
E. Penyedia elektron
Kunci Jawaban: A
Pembahasan:
Istilahnya saja perlindungan katodik, jadi apa yang dilindungi? Pasti katodanya. Sehingga katoda adalah bahan yang dilindungi dari perkaratan.
16. Pada Teknik perlindungan katodik, anoda dipilih dari logam yang memenuhi spesifikasi berikut …
A. lebih murah dari besi
B. lebih kuat dari besi
C. lebih tahan karat dari besi.
D. potensial reduksi lebih kecil dari pada besi.
E. lebih mudah memuai dari pada besi
Kunci Jawaban: D
Pembahasan:
Pada cara perlindungan katodik ada acara pengorbanan anoda. Dalam cara ini dipilih anode dari bahan yang mempunyai potensial reduksi lebih kecil dari besi agar anode tersebut yang mengalami oksidasi bukan besi
B. Latihan Soal Pilihan Ganda Kimia Kelas 12 Bab 5 Korosi
Disclaimer:
Kunci Jawaban ada di akhir soal Pilihan Ganda. Gunakan Kunci Jawaban yang ada sebagai alternatif jawaban soal. Jika ada kekeliruan atau keraguan, silahkan diskusikan dengan guru PJOK di kelas kalian. Semangat belajar.
Jawablah soal-soal berikut ini dengan memilih huruf A, B, C, D, atau E pada jawaban yang benar dan tepat!
1. Logam-logam berikut yang paling tahan terhadap korosi adalah …
A. Cr
B. Ni
C. Zn
D. Fe
E. Cu
2. Faktor utama dalam proses perkaratan besi adalah …
A. Zat asam
B. Gas oksigen
C. Ion H+
D. Besi
E. udara
3. Souvenir dari bahan logam yang paling awet tidak mengalami korosi adalah terbuat dari
A. Aluminium
B. Besi
C. Tembaga
D. Perak
E. Paduan logam perunggu
4. Dalam peristiwa perkaratan besi, gas oksigen bertindak sebagai …
A. Anoda
B. Katoda
C. Jembatan garam
D. Elektrolit
E. Katalis
5. Peristiwa perkaratan logam merupakan sel galvani alami karena …
A. Menghasilkan potensial sel negatif.
B. Merupakan reaksi spontan oleh alam
C. Terdapat kation dan anion.
D. Terjadi reaksi redoks.
E. Disebabkan oleh lingkungan.
6. Tingkat kerusakan struktur bangunan akibat perkaratan besi lebih banyak terjadi pada …
A. Bagunan daerah rawa
B. Bagunan daerah kota
C. Bangunan daerah mangrove
D. Bangunan daerah gunung
E. Bangunan daerah hutan
7. Perhatikan percobaan tentang perkaratan logam besi berikut
Peristiwa perkaratan paling lambat terjadi pada percobaan nomor …
A. 1
B. 2
C. 3
D. 4
E. 5
8. Salah satu cara mencegah terjadinya reaksi korosi pada menara adalah . . . .
A. Dilapisi timah.
B. Direndam dengan air.
C. Dibakar lalu ditempa.
D. Dicelupkan pada larutan asam.
E. Dihubungkan dengan lempeng magnesium.
9. Seng dipilih sebagai pelapis besi untuk mencegah terjadinya korosi karena . . . .
A. Besi menjadi anode.
B. Seng menjadi katode.
C. Harga E0 besi lebih besar.
D. Harga E0 besi dan seng sama.
E. Besi menjadi mudah teroksidasi.
10. Diketahui :
Fe2+ (aq) + 2e
Fe(s) E0 = - 0,44 Volt
Ni2+ (aq) + 2e
Ni(s) E0 = - 0,25 Volt
Mg2+ (aq) + 2e
Mg(s) E0 = - 2,37 Volt
Cu2+ (aq) + 2e
Cu(s) E0 = + 0,34 Volt
Ag+
(aq) + e
Ag(s) E0 = + 0,80 Volt
Pb2
+(aq) + 2e
Pb(s) E0 = - 0,13 Volt
Logam yang dapat melindungi besi dari perkaratan dengan perlindungan katodik adalah . . . . .
A. Ni
B. Mg
C. Cu
D. Ag
E. Pb
11. Perlindungan korosi yang paling tepat dilakukan untuk melindungi logam pada bagian mesin yang berputar adalah ….
A. Mengecat
B. dibuat paduan logam
C. perlindungan katodik
D. melumuri dengan oli
E. dibalut dengan emas
12. Di daerah industri, gas-gas yang dapat menyebabkan korosi adalah …
A. O2 dan N2
B. CO dan H2O
C. CO dan N2
D. SO2 dan NO2
E. CO2 dan CO
13. Pada peristiwa korosi, besi mengalami oksidasi, sedangkan yang mengalami reduksi adalah …
A. H+
B. O2
C. Fe2+
D. OHE. H2O
14. Untuk kepentingan konstruksi jembatan, dibutuhkan logam besi yang kuat. Maka Teknik pelapisan logam besi yang tepat adalah menggunakan …
A. Timah
B. Nikel
C. Seng
D. Crom
E. Tembaga
15. Pelapisan besi menggunakan plastik lebih cocok digunakan pada alat …
A. Alat rumah tangga
B. Onderdil sepeda motor
C. Kerangka jembatan
D. Alat memasak
E. Kerangka rumah
Jawaban Latihan Soal Pilihan Ganda Kimia Kelas 12 Bab 5 Korosi
1.
E
2.
B
3.
D
4.
B
5.
B
6.
C
7.
D
8.
E
9.
C
10.
B
11.
D
12.
D
13.
B
14.
C
15.
A
Demikian postingan Sekolahmuonline yang menyajikan contoh soal pilihan ganda atau multiple choice mata pelajaran Kimia kelas 12 Bab Korosi. Soal Sekolahmuonline rujuk dari Modul PJJ dengan dikemas lagi agar lebih memudahkan untuk dibaca dan dipelajari. Semoga bermanfaat, silahkan baca-baca postingan Sekolahmuonline yang lainnya. Selamat dan semangat belajar. Semoga masa depan Anda tercerahkan.
Baca juga soal-soal dan rangkuman mata pelajaran Kimia kelas 12 pada postingan di bawah ini:
Soal-soal Kimia kelas 12 lengkap dengan kunci jawaban dan pembahasannya:
- Contoh Soal PG Kimia Kelas 12 Bab 1 Sifat Koligatif Larutan Beserta Jawabannya
- Contoh Soal Kimia Kelas 12 Bab 1 Sifat Koligatif Larutan Beserta Jawaban atau Pembahasannya
- Contoh Soal Kimia Kelas 12 Bab 3 Deskripsi Unsur-Unsur Golongan Utama
- Soal Pilihan Ganda Kimia Kelas 12 Bab 4 Sel Volta dan Aplikasinya dalam Kehidupan
- Soal Kimia Kelas 12 Bab 5 Korosi
- Sebutkan kegunaan Karbon Dioksida
Rangkuman atau ringkasan Kimia Kelas 12:
- Rangkuman Kimia Kelas 12 Bab 1 Sifat Koligatif Larutan
- Rangkuman Kimia Kelas 12 Bab 2 Elektrokimia
- Rangkuman Kimia Kelas 12 Bab 3 Deskripsi Unsur-Unsur Golongan Utama
- Rangkuman Kimia Kelas 12 Bab 4 Sel Volta dan Aplikasinya dalam Kehidupan
- Rangkuman Kimia Kelas 12 Bab 5 Korosi
- Rangkuman Kimia Kelas 12 Bab 6 Sel Elektrolisis