Soal Kimia Kelas 11 Bab Pergeseran Kesetimbangan + Kunci Jawabannya ~ sekolahmuonline.com
Soal Kimia Kelas 11 Bab Pergeseran Kesetimbangan + Kunci Jawabannya ~ sekolahmuonline.com. Pembaca Sekolahmuonline, berikut Sekolahmuonline sajikan contoh soal mata pelajaran Kimia Kelas XI Bab Pergeseran Kesetimbangan lengkap dengan kunci jawabannya. Silahkan dibaca dan dipelajari, semoga membantu mempermudah pembaca Sekolahmuonline semuanya dalam Kimia secara mandiri khususnya Bab Pergeseran Kesetimbangan.
Kimia Kelas 11 Bab Pergeseran Kesetimbangan membahas satu Kegiatan Pembelajaran yang meliputi pembahasan tentang: Azas Le Chatelier, Faktor–faktor yang Mempengaruhi Pergeseran Kesetimbangan dan Penerapan Kesetimbangan di Industri.
Contoh Soal Kimia Kelas XI Bab Pergeseran Kesetimbangan
Sebelum masuk ke soal-soal Kimia Kelas XI Bab Pergeseran Kesetimbangan, silakan baca istilah-istilah yang mungkin akan sering Anda jumpai ketika membahas Bab ini. Sehingga, Anda menjadi tidak asing lagi dengan istilah-istilah yang ada. Hal ini tentu akan memudahkan Anda dalam mempelajari Kimia khususnya Bab Pergeseran Kesetimbangan.
- Kesetimbangan Dinamis :
Suatu keadaan dari sistem kesetimbangan yang menyatakan reaksi terus berlangsung ke dua arah yang berlawanan secara mikroskopis
- Azas Le Chatelier :
Prinsip yang menyatakan bahwa jika dalam suatu sistem kesetimbangan mengalami perubahan konsentrasi, suhu,
volume, atau tekanan maka sistem akan menyesuaikan dirinya untuk meniadakan pengaruh perubahan yang diterapkan hingga kesetimbangan baru tercapai
- Konsentrasi larutan :
Besaran yang menunjukkan kepekatan suatu larutan melalui perbandingan antara zat terlarut dan pelarut
- Koefisien Reaksi
: Angka yang ditulis mendahului rumus kimia zat, yang menyatakan perbandingan mol zat yang terlibat dalam reaksi
- Reaksi Eksoterm
:
Reaksi yang melepaskan kalor dari sistem ke lingkungan sehingga entalpi hasil reaksi menjadi berkurang
- Reaksi Endoterm :
Reaksi yang menyerap kalor dari lingkungan ke sistem sehingga entalpi hasil reaksi bertambah
- Kalor
:
Energi yang berpindah akibat adanya perbedaan suhu
- Entalpi
: Jumlah energi yang terkandung dalam suatu materi
- Proses Haber Bosh
:
Proses pembuatan gas amonia di industri yang menggunakan bahan baku gas nitrogen dan gas oksigen dengan katalis besi (Fe)
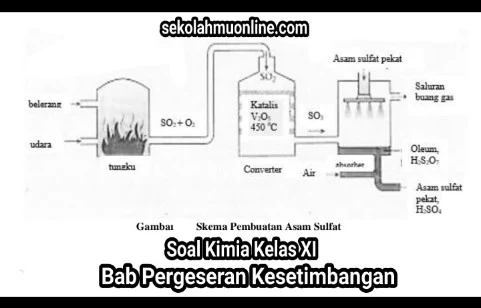
- Proses Kontak :
Proses pembuatan asam sulfat di industri dengan menggunakan katalis vanadium pentaoksida (V2O5)
- Katalis
:
Zat yang dapat mempercepat terjadinya reaksi tetapi tidak ikut bereaksi
- Optimal
:
Suatu kondisi tertinggi dari suatu proses
Soal Pilihan Ganda Kimia Kelas 11 Bab Pergeseran Kesetimbangan
Nah, berikut ini contoh soal pilihan ganda Kimia kelas XI Bab Pergeseran Kesetimbangan lengkap dengan kunci jawaban dan pembahasannya. Silakan dibaca dan dipelajari. Selamat belajar. Jika ada kesulitan atau merasa jawaban yang ada salah, silakan diskusikan dengan Guru Kimia di kelas Anda.
Catatan: Berhubung penulisan angka/simbol/dll tertentu tidak dapat tercover dengan Handphone, silakan lihat soal dan jawaban pada screenshot/capture.
Jawablah soal-soal di bawah ini dengan memilih huruf A, B, C, D, atau E pada jawaban yang benar dan tepat!
1. Agar pada reaksi kesetimbangan:
N2(g) + O2(g) ⇌ 2NO(g) ∆H = +180 kj
Jumlah gas NO yang dihasilkan maksimal, maka tindakan yang diperlukan adalah…
A. Menaikan tekanan
B. Menurunkan tekanan
C. Mengecilkan volum
D. Menaikkan suhu
E. Memperbesar volume
Kunci Jawaban: B
Pembahasan:
Menurut Azas Le Chatelier, jika sistem dalam kesetimbangan terjadi kenaikan suhu, maka akan terjadi pergeseran kesetimbangan kearah reaksi yang menyerap kalor (Apabila koefisien sama antara produk dan reaksi maka volume dan tekanan tidak mempengaruhi reaksi. Reaksi diatas termasuk reaksi endoterm jadi jika dinaikkan suhu maka kesetimbangan akan bergeser kearah reaksi endoterm atau bergeser kearah kanan (NO), jika reaksi bergeser kerah kanan maka nilai Kc akan semakin besar.
2. Perhatikan reaksi berikut.
2N2O5(g) ⇌ 4NO2(g) + O2(g) ∆H = –T kkal
Reaksi kesetimbangan bergeser kekiri jika…
A. Konsentrasi O2 ditambah
B. Suhu diturunkan
C. Tekanan diperkecil
D. Konsentrasi NO2 dikurangi
E. Volume diperbesar
Kunci Jawaban: B
Pembahasan:
Jika suhu diturunkan reaksi kesetimbangan bergeser ke
kiri. Jika suhu dinaikkan reaksi kesetimbangan bergeser ke kanan.
3. Perhatikan reaksi kesetimbangan berikut:
2NO(g) + O2(g) ⇌ 2NO2(g) ∆H +150 kj
Apabila pada volume tetap pada temperatur dinaikkan, kesetimbangan bergeser kearah…
A. Kanan dan harga K tetap
B. Kiri dan harga K kecil
C. Kanan dan harga K semakin besar
D. Kanan dan harga K semakin kecil
E. Kiri dan harga K makin besar
Kunci Jawaban: C
Pembahasan:
Kenaikan temperatur menyebabkan kesetimbangan bergeser kekanan, kearah hasil dan harga K naik
4. Berikut adalah faktor-faktor yang mempengaruhi kesetimbangan suatu reaksi reversibel, kecuali….
A. Suhu
B. Volume
C. Tekanan
D. Konsentrasi
E. Katalisator
Kunci Jawaban: E
Pembahasan:
Faktor-faktor yang mempengaruhi kesetimbangan yaitu suhu, konsentrasi, tekanan, dan volume.
5. jika terhadap suatu sistem kesetimbangan dilakukan suatu aksi, pada system akan terjadi suatu reaksi sehingga pengaruh aksi terhadap system menjadi sekecil mungkin. Asas ini dikemukakan oleh . . . . .
A. Van’t Haff
B. de Broglie
C. Le Chatelier
D. Hess
E. Dalton
Kunci Jawaban: C
Pembahasan:
Hubungan antara reaksi yang timbul pada system kesetimbangan dengan aksi yang diberikan dari luarvdirumuskan oleh seorang ahli kimia berkebangsaan perancis, Henry Louis Le Chatelier, yang tekenal dengan asas Le Chatelier, yang menyatakan:
“Jika pada suatu sistem yang berada dalam keadaan setimbang dilakukan suatu aksi (tindakan), maka system akan mengadakan reaksi yang cenderung mengurangi pengaruh aksi tersebut.”
6. Diantara persamaan reaksi kesetimbangan berikut ini akan bergeser ke kanan jika tekanan diperbesar, yaitu . . .
A. S(s) + O2(g) ⇌ SO2(g)
B. H2(g) + I2(g) ⇌ 2 HI(g)
C. 2 SO3(g) ⇌ 2 SO2(g) + O2(g)
D. C(s) + O2(g) ⇌ CO2(g)
E. N2(g) + 3H2(g) ⇌ 2 NH3(g)
Kunci Jawaban: E
Pembahasan:
Dapat kita lihat bahwa pada persamaan reaksi:
N2(g) + 3H2(g) ⇌ 2NH3(g)
jumlah mol diruas kiri (4) > jumlah mol diruas kanan (2)
Kemudian jika tekanan diperbesar maka volume akan berkurang, reaksi akan bergeser kejumlah mol yang paling kecil yaitu pada ruas kanan. Jadi, reaksi akan bergeser ke arah kanan.
7. Reaksi homogen yang tidak dipengaruhi oleh perubahan volume adalah…
A. 2NO2(g) ⇌ 2 NO(g) + O2(g)
B. 2 NH3(g) ⇌ N2(g) + 3 H2(g)
C. PCl5(g) ⇌ PCl3(g) + Cl2(g)
D. 2 HCl(g) ⇌ H2(g) + Cl2(g)
E. H2(g) + I2(g) ⇌ 2 HI(g)
Kunci Jawaban: D
Pembahasan:
Bila volume diperbesar kesetimbangan akan bergeser menuju keruas dengan jumlah molekul atau partikel (jumlah koefisien reaksi ) yang besar.
Jadi, pada reaksi
2HCl(g) ⇌ H2(g) + Cl2(g) jumlah koefisien pada ruas kiri dan kanan yaitu sama sehingga tidak dipengaruhi oleh volume.
8. Pada reaksi kesetimbangan: N2(g) + 3H2(g) ⇌ 2NH3(g) ∆H = – x kJ
Jika suhu diturunkan, kesetimbangan akan bergeser ke ….
A. kiri, karena proses reaksi eksoterm
B. kiri, karena ∆H = – x kJ
C. tetap, karena jumlah koefisien reaksi pereaksi lebih besar
D. kanan, karena proses reaksi berlangsung eksoterm
E. kanan, karena proses reaksi endoterm
Kunci Jawaban: D
Pembahasan:
Reaksi kesetimbangan pada soal ini bersifat eksoterm (menghasilkan kalor) maka jika suhu diturunkan kesetimbangan bergeser ke kanan karena proses reaksinya berlangsung eksoterm.
9. Reaksi kesetimbangan
2NO(g) + O2(g) ⇌ 2NO2(g) ∆H = –27 kJ
Jika volume diperbesar, kesetimbangan akan bergeser ke ….
A. kanan, gas NO2 berkurang
B. kanan, gas NO2 bertambah
C. kanan, gas NO bertambah
D. kiri, gas NO bertambah
E. kiri, gas NO berkurang
Kunci Jawaban: D
Pembahasan:
Karena yang diubah adalah faktor volume diperbesar maka sistem kesetimbangan reaksi soal ini akan bergeser ke sisi di mana jumlah molekulnya lebih besar (dalam hal ini ke sisi pereaksi ~ kiri) dan gas NO menjadi bertambah.
10. Pada reaksi kesetimbangan: 2SO2(g) + O2(g) ⇌ 2SO3(g) ∆H = – y kJ
Jika volume diperkecil, kesetimbangan akan bergeser ke ….
A. kiri, karena ke arah eksoterm
B. kanan, karena ke arah endoterm
C. kiri, karena jumlah koefisien pereaksi lebih besar
D. kanan, karena proses reaksi eksoterm
E. kanan, karena jumlah koefisien hasil reaksi lebih kecil
Kunci Jawaban: E
Pembahasan:
Karena yang diubah adalah faktor volume yang diperkecil maka sistem kesetimbangan reaksi soal ini akan bergeser ke sisi di mana jumlah molekulnya lebih sedikit (diindikasikan dengan jumlah koefisien zat), sisi kanan jumlah koefisiennya lebih kecil, dalam hal ini ke sisi hasil reaksi ~ kanan.
Screenshot Soal Pilihan Ganda Kimia Kelas 11 Bab Pergeseran Kesetimbangan dan Kunci Jawabannya
Berikut ini capture/screenshot soal yang dapat Anda gunakan untuk mengecek secara langsung simbol-simbol, angka, dll yang tepat. Semoga membantu mempermudah dan sekaligus mengoreksi kekeliruan yang ada.
Demikian postingan Sekolahmuonline yang menyajikan Contoh Soal Pilihan Ganda Kimia Kelas XI Bab Pergeseran Kesetimbangan Lengkap dengan Kunci Jawabannya. Semoga bermanfaat. Silakan baca-baca postingan Sekolahmuonline yang lainnya.
Kumpulan Rangkuman Kimia Kelas XI
Lengkap Rangkuman atau Ringkasan Kimia kelas XI semua Bab silakan pembaca Sekolahmuonline lihat pada tautan/link yang ada di bawah ini. Jika ada tautan/link yang error/mati, silakan beritahukan kepada kami langsung lewat kolom komentar atau lewat kontak yang sudah disediakan untuk segera Sekolahmuonline perbaiki.
- Rangkuman Kimia Kelas 11 Bab Senyawa Hidrokarbon ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Minyak Bumi ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Dampak Reaksi Pembakaran Hidrokarbon ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Konsep Dasar Perubahan Entalpi ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Jenis-jenis dan Cara Penentuan Entalpi Reaksi ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Faktor-Faktor yang Mempengaruhi Laju Reaksi dan Teori Tumbukan ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Laju Reaksi ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Kesetimbangan Kimia ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Pergeseran Kesetimbangan ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Larutan Asam dan Basa ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Hidrolisis Garam ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Larutan Penyangga ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Titrasi Asam Basa ~ sekolahmuonline.com
- Rangkuman Kimia Kelas 11 Bab Sistem Koloid ~ sekolahmuonline.com
Kumpulan Soal Kimia Kelas XI
Lengkap soal-soal Kimia kelas XI dan kunci jawaban serta pembahasannya dari semua Bab yang ada, silakan pembaca Sekolahmuonline lihat pada tautan/link yang ada di bawah ini. Jika ada tautan/link yang error/mati, silakan beritahukan kepada kami langsung lewat kolom komentar atau lewat kontak yang sudah disediakan untuk segera Sekolahmuonline perbaiki.
- Soal Kimia Kelas 11 Bab Senyawa Hidrokarbon ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Minyak Bumi ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Dampak Reaksi Pembakaran Hidrokarbon ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Konsep Dasar Perubahan Entalpi ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Jenis-jenis dan Cara Penentuan Entalpi Reaksi ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Faktor-Faktor yang Mempengaruhi Laju Reaksi dan Teori Tumbukan ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Laju Reaksi ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Kesetimbangan Kimia ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Pergeseran Kesetimbangan ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Larutan Asam dan Basa ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Hidrolisis Garam ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Larutan Penyangga ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Titrasi Asam Basa ~ sekolahmuonline.com
- Soal Kimia Kelas 11 Bab Sistem Koloid + Kunci Jawabannya ~ sekolahmuonline.com